简介
细胞因子诱导的杀伤细胞(CIK)最早发现于1991年[1],是一种异质性的CD8+T细胞群,由人外周血淋巴细胞(PBLs)产生,并通过注入抗CD3抗体、干扰素-γ (IFN-γ)和白介素(IL)-2等细胞因子进行孵育,实现体外扩增。它们能杀灭由凋亡相关因子配体(FASL)和穿孔素[2]介导的肿瘤细胞。
CIK细胞可以通过激活NK细胞受体,如DNAX辅助分子-1、NKp46、NKG2D、NKp30等,以非主要组织兼容性复合体(MHC)限制性的方式裂解癌细胞[3-5]。除了对癌细胞有直接杀伤作用外,CIK细胞还可以通过分泌多种细胞因子来调节免疫功能。大量研究表明,CIK细胞受肿瘤细胞刺激后,其分泌的促炎因子如肿瘤坏死因子(TNF)-α、IFN-γ、IL-2等水平显著上调[6],这些细胞因子进一步增强全身抗肿瘤活性,诱导Th1免疫应答。
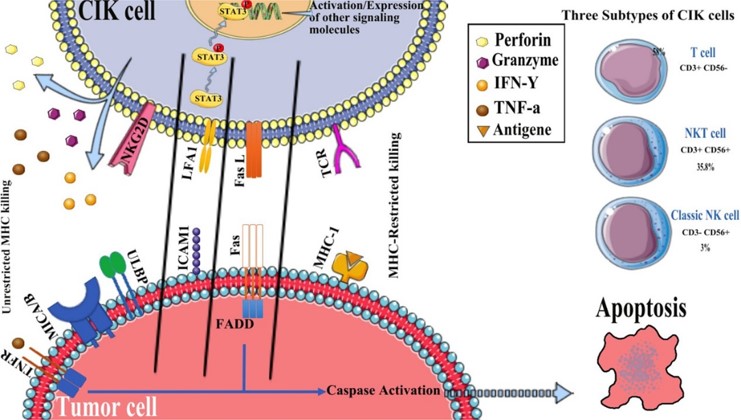
图 1 :CIK 细胞毒性的可能机制。作为多种细胞的混合,CIK 包括 T 细胞 (CD3+CD56-)、NK-T 细胞 (CD3+CD56+) 和 NK 细胞群 (CD3-CD56+)。
作用机理
目前,关于 CIK 细胞的细胞毒性的信息还比较少,其确切机制尚未完全阐明。阻断白细胞功能相关的抗原-1 和细胞间粘附分子-1 的单克隆抗体抑制 CIK 细胞的细胞毒作用。结果,CIK细胞在肿瘤细胞裂解的介导下发生细胞间的接触。[7]。
在CIK细胞对肿瘤的识别过程中,发挥最重要作用的分子可能是自然杀手2组的成员:D (NKG2D)受体。NKG2D是c型凝集素激活受体家族的一员,在进化上较为保守,位于人类染色体12p12-p13上的NK基因复合物之中[8]
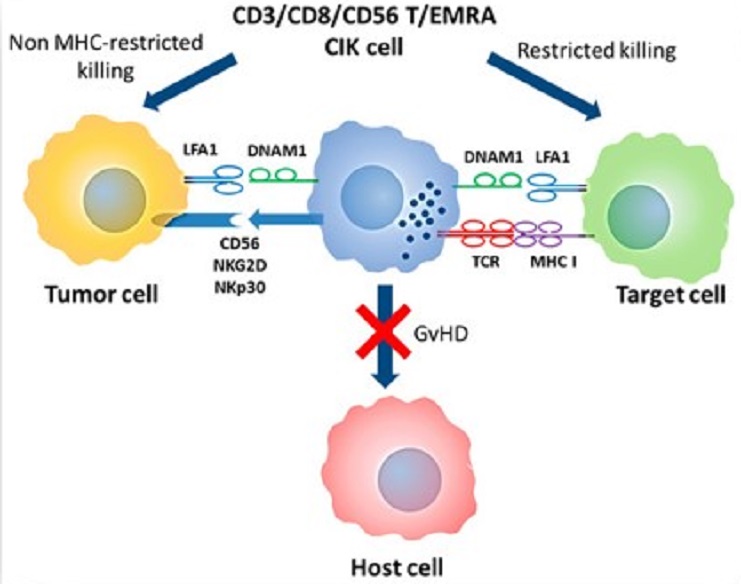
图 2: CIK 细胞的双 T/NK 特异性和作用机制。CIK 细胞是T-EMRA 淋巴细胞,它保持着原始 TCR的特异性并获得NK样细胞毒性。不论哪种情况,DNAM1和LFA1都是靶标结合所必需的,而NK样细胞毒性由CD56、NKp30和NKG2D分子所介导。
癌症类型
VAMOS与台中童综合医院及马来西亚各私立医院合作,经台湾卫生福利部和马来西亚卫生部批准,参与了多项细胞疗法(DC、CIK、DC-CIK细胞疗法)在多种实体癌治疗项目中的应用。
所参与的细胞治疗应用涵盖 22 种类型的 4 期实体癌,具体类型如下 [参考:MOHW,台湾]:
- 肾上腺癌
- 胆道癌
- 膀胱癌
- 脑恶性肿瘤
- 乳腺癌
- 宫颈癌
- 结直肠癌
- 子宫内膜癌
- 食道癌
- 胃癌
- 生殖细胞癌
- 头颈癌
- 肾癌
- 肝癌
- 肺癌
- 神经内分泌癌
- 卵巢癌
- 胰腺癌
- 前列腺癌
- 软组织肉瘤
- 皮肤癌
- 甲状腺癌
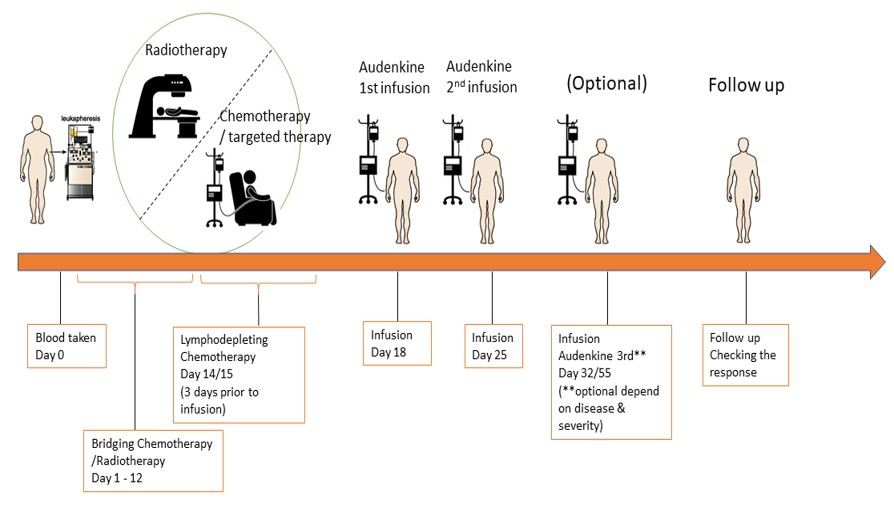
治疗流程
用法

仅限自体回输。患者将接受至少 2个周期的 CIK细胞输注,每个周期之间间隔一周。5~7 x109的细胞配成240mL生理盐水悬液,30-45分钟内静脉滴注给药。
免疫细胞治疗可以结合其他疗法联用,包括抗炎药(NSAID)和解热镇痛药,以缓解患者的不适。DC细胞疗法也可联合放疗、靶向治疗、化疗、免疫检查点抑制剂治疗等,提高整体抗癌疗效。所有联用治疗方法必须由医疗专家根据临床经验进行评估,并随时观察联合治疗过程中的不良反应。
患者出院后应进行随访,包括血常规检查和PET CT/CT筛查,前2年每3个月一次,随后3年每6个月一次,第5年起每年一次。
可能的副作用
据临床试验文献记载,CIK细胞治疗最常见的不良反应多为发热、疼痛等轻微症状。虽然其发生频率非常低,并且在未经额外治疗的情况下自行消退,但不同患者可能因个体差异和特殊体质而产生特殊(特异性)反应。如果细胞回输后出现恶心、呕吐、腹泻或休克,应停止细胞回输,并遵照医生指示进行治疗。
| 不良反应 | 描述 |
|---|---|
| 1级 | 手术医师需要将患者置于舒适空间加以观察,直至不良反应自行消退,或给予适当支持(冰敷、喝温水、睡眠等)。 |
| 2级 | 手术医师应立即安置患者,并观察不良反应是否趋于缓解,或者变得更严重。如果趋于缓解,则给予物理支持,加速不良反应的消退;如果趋于严重,则评估患者不良反应的严重程度,并给予适当的药物支持(解热、镇痛、类固醇等)。继续观察并给予药物支持,直到不良反应稳定或消失。暂停DC细胞治疗,进入观察期,查明原因后再评估是否继续治疗。 |
| 3级 | 手术医师必须立即采取紧急措施,并根据患者症状给予药物支持(解热、镇痛、类固醇、增压、电解质输注,等等)。安排住院并持续治疗,缓慢减药直至症状完全消失。患者退出该DC细胞疗程,终止细胞回输,并为患者安排常规医疗护理。 |
| 4级 | 手术医师必须立即将患者送往急诊科,根据患者症状采取急救措施,并提供生命支持(气管插管、类固醇、增压、电解质输注等)。尽快安排到重症监护室继续治疗,直到症状完全稳定或消退。患者退出该DC细胞疗程,终止细胞回输,并为患者安排常规医疗护理。 |
实验室制备工艺
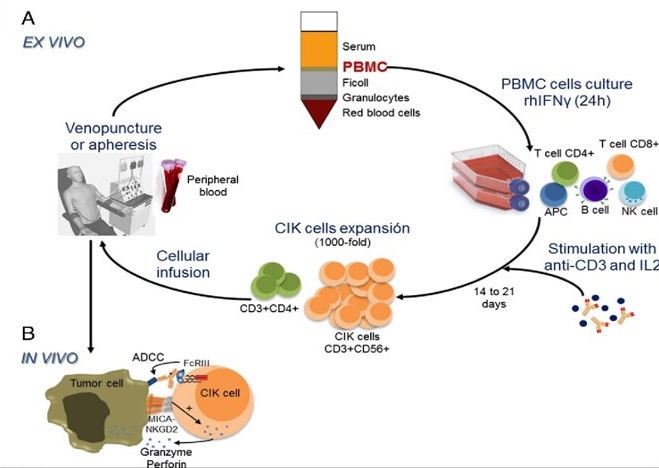
图中为实验室中CIK细胞的生产过程。在医院通过单采收集患者的PBMC细胞,并通过专业快递服务(全球速递)直接发送到我们在马来西亚的实验室。收到PBMC样品后,我们将立即准备进行分离和细胞计数。然后使用含有1000 Uml IFN-g的无血清培养基,在370℃、5% CO2、95%相对湿度下培养细胞24小时。24小时后,在培养基中加入抗CD3抗体(最终浓度为100 ngml)、1 ngml IL-1a和1000 Uml重组的IL-2。培养 14 天后,自体 CIK 细胞在 240 ml 生理盐水中制成悬液。然后,将细胞转移到临床级细胞培养袋中。细胞产品按照现行的《中国药典》规定进行检测,例如进行微生物污染检测以确保可靠性,进行基于PCR的支原体检测方法排除污染,并通过动力学比浊法定量细菌内毒素。通过QC质检后,细胞产品冷冻保存并运送到医院。医院完成提取后,CIK细胞即可进行回输。
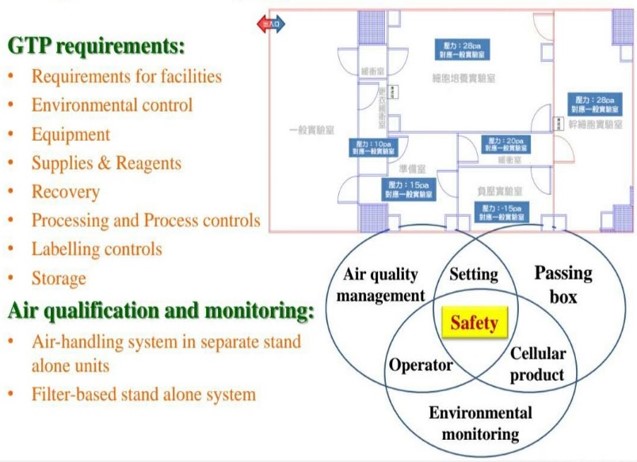
人体细胞组织优良操作规范(GTP)实验室

我们的实验室设计遵循的规范比任何人体细胞组织优良操作规范(GTP)都要更为严格,包括多次更衣程序(第一、第二更衣室、生物安全区、合格人员的有限访问),全面避免了环境污染风险。实验室设施符合 FDA 高标准二次更衣设施要求。

场地规格
达到万级洁净度,“正压、恒湿、恒温”的高标准无尘独立实验室,设有完整的控制机制,可提供各种工艺设施为细胞治疗所用。
洁净度
万级洁净度,完善的控制机制,可提供细胞治疗所需的各种工艺设施。
严苛要求
坚持使用从优质厂家采购的试剂,使用高端设备,全流程无血清培养,提高人体细胞组织的操作有效性和安全性。为人体细胞组织的接收/培养、验收/退回、分发、销毁或处置等操作建立了严苛的操作程序、制造程序、储存条件、有效期和记录存档。



全方位支持
- 患者培训材料
- 医生培训材料
- 免费的疗前评估
- 在马来西亚的治疗将提供全面的辅助支持
- 疗后监测
补充阅读
演示文稿
科学出版物
| 年 | 杂志 | 科学研究 |
|---|---|---|
| 2019 | Lancet Haematol 杂志 | 人源化抗CD19和抗BCMA CAR T细胞联合治疗复发或难治性多发性骨髓瘤患者;单臂 2 期试验 |
| 2017 | Wiley AJH | 人源化 CD19 靶向嵌合抗原受体 T (CAR-T) 细胞在复发难治性急性淋巴细胞白血病患者中的强效抗白血病活性 |
| 2019 | 《细胞疗法》 | 抗 CD19 嵌合抗原受体 T 细胞对 B 细胞恶性肿瘤的疗效 |
| 2019 | 期刊:《分子疗法杂志》 | 在晚期实体癌中识别间皮素的慢病毒转导 CAR 修饰的 T 细胞的 I 期研究 |
| 2019 | 《临床肿瘤学》杂志 | Claudine 18.2 的 1 期试验——用于晚期胃癌和胰腺癌的特异性 CAR-T 细胞 |
| 2017 | 《临床肿瘤学》杂志 | 抗GP3嵌合抗原受体修饰T细胞(GP3 CAR-T)在中国难治性或复发性GPC3+肝细胞癌(r/r GP3+ HCC)患者中的一期研究 |
| 2016 | 《新英格兰医学杂志》 | 嵌合抗原受体 T 细胞治疗后胶质母细胞瘤的消退 |
| 2016 | 期刊:《血液评论》 | 嵌合抗原受体 T 细胞疗法:酝酿 25 年 |
Vamos 的生命细胞疗法
早在2016年,VAMOS就开始从事生命细胞疗法。我们为那些寻求最有效癌症治疗的医院和患者提供尖端的生物技术产品。VAMOS的T细胞免疫治疗和服务极其精确和个性化,我们始终专注提供最高质量标准、最具性价比、最有效的治疗方案。
VAMOS 服务
我们提供以下服务:
- 为马来西亚国内外医院制备和供应用于 CAR-T 治疗的自体 CAR-T 细胞。
- 接待在马来西亚接受 CAR-T 治疗的国际患者,以及相关医疗旅游和辅助服务。
关于VAMOS的一些事实
- 我们是马来西亚唯一一家针对白血病的CAR-T疗法供应商。
- 我们的CAR-T疗法经过马来西亚卫生部批准。
- 所有参与我们临床试验的患者都得到完全缓解,癌症消失(除了3名患者在接受CAR-T治疗前去世)。
- 6 家马来西亚顶级医院使用我们的产品进行CAR-T治疗。
- 到目前为止,我们已经治疗了100多位4期癌症患者,CAR-T治疗成功率超过90%。
- 迄今为止,所有接受我们CAR-T治疗的患者均已获得成功治疗,且未出现任何严重副作用。
- 我们的 CAR-T 疗法的质量首屈一指,而成本可能是全球医疗保健领域最低。
- 除CIK疗法外,我们还提供针对实体癌的DC和DC-CIK疗法,以及针对白血病和实体癌的CAR-T疗法。

参考文献
- Schmidt-Wolf IG、Negrin RS、Kiem HP、 Blume KG、Weissman IL,使用 SCID 小鼠/人淋巴瘤模型评估具有有效抗肿瘤细胞活性的细胞因子诱导的杀伤细胞,《实验医学》杂志 (1991) 174(1):139–49. doi:10.1084/jem.174.1.139
- Lee HK、Kim YG、Kim JS、Park EJ、Kim B、Park KH, 等,细胞因子诱导的杀伤细胞通过CCR5 信号传导与肿瘤裂解物冲击的树突细胞的相互作用,《肿瘤通讯》杂志 (2016) 378(2):142–9. doi:10.1016/j.canlet.2016.05.020
- Verneris MR、Karimi M、Baker J、Jayaswal A、Negrin RS,NKG2D 信号在激活和扩增的 CD8+ T细胞的细胞毒性中的作用,《血液》杂志 (2004) 103(8):3065–72. doi:10.1182/blood-2003-06-2125
- Schmidt TL、Negrin RS、Contag CH,癌症免疫疗法的杀手级选择。《免疫学研究》杂志 (2014) 58(2–3):300–6。 doi:10.1007/s12026-014-8507-2
- Pievani A、Belussi C、Klein C、Rambaldi A、Golay J、Introna M,联合使用细胞因子诱导的杀伤细胞(CIK)和抗CD20抗体增强对人B细胞淋巴瘤靶点的杀伤,《血液》杂志 (2011) 117(2):510–8. doi:10.1182/blood-2010-06-290858
- Linn YC、Wang SM、Hui KM,使用寡核苷酸阵列对细胞因子诱导的杀伤细胞响应急性髓系白血病和急性淋巴细胞白血病刺激物的基因表达谱比较分析,《实验血液学》杂志 (2005) 33(6):671–81. doi:10.1016/j.exphem.2005.03.005
- Solmaz Shirjang、Nazila Alizadeh、Behzad Mansoori、Ata Mahmoodpoor、Hossein Samadi Kafil、Mohammad Hojjat‐Farsangi、 Mehdi Yousefi,前景光明的免疫疗法:异军突起的细胞因子诱导的杀伤细胞,《细胞生物化学》杂志2018;1-21. doi: 10.1002/jcb.28250
- Martino Introna、Fabio Correnti,CIK 细胞给癌症患者带来崭新的临床前景,《Int. J. Mol.Sci》杂志,2018, 19(2), 358. https://doi.org/10.3390/ijms19020358
